孙涛垒教授团队在CEJ上发表纳米材料调控淀粉样蛋白自组装最新研究成果
近日,武汉理工大学神经退行性疾病纳米医药湖北省重点实验室孙涛垒教授团队在化工领域顶级期刊《Chemical Engineering Journal》(IF:13.3,中科院一区top 期刊)上发表最新研究成果,提出了一种基于非共价相互作用的纳米生物界面设计准则,为开发抑制淀粉样蛋白(如阿尔茨海默病中的Aβ肽)异常聚集的纳米药物提供了理论和技术支持。该研究通过精确调控纳米复合材料界面能量,首次揭示了其影响淀粉样蛋白自组装与纤维分解的分子机制,并验证了相关设计标准的普适性。
阿尔茨海默病等神经退行性疾病与淀粉样蛋白(如Aβ肽)的异常折叠及纤维化密切相关。现有研究多聚焦于人工纳米材料模拟“分子伴侣”的功能,通过非共价相互作用稳定蛋白质稳态,但缺乏统一的设计标准。本研究以零维纳米颗粒与二维纳米片复合结构(NPs@NSs)为模型,系统解析了纳米生物界面能量效应对淀粉样蛋白行为的影响。
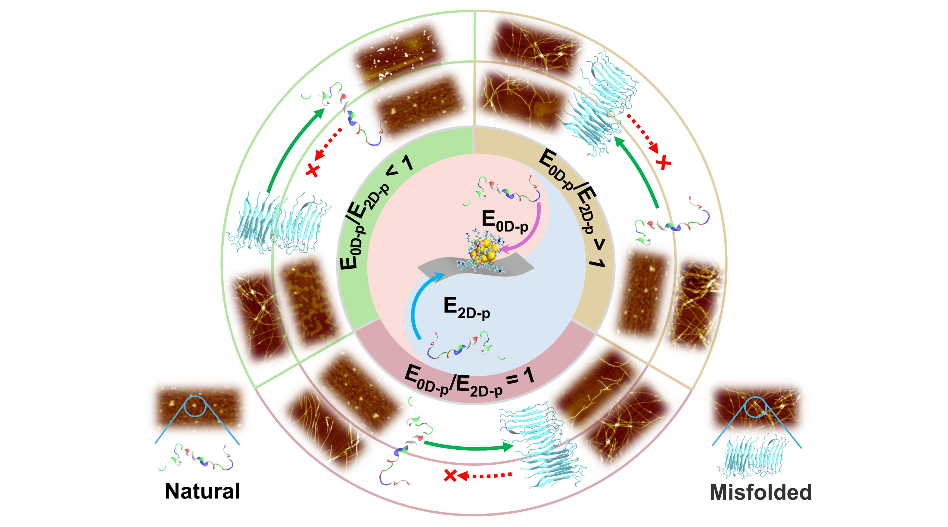
基于非共价相互作用的纳米生物界面设计准则示意图
研究团队通过分子动力学模拟和实验验证,提出了“非共价界面亲和能比值(E0D-p/E2D-p)”的核心指标。当0D纳米颗粒与2D纳米片对Aβ肽的亲和能比值小于1时(如AuNCs@rGO和AuNCs@BP),复合材料能通过双位点协同作用稳定Aβ单体天然构象,并破坏成熟纤维的β-折叠结构;而当该比值接近或大于1时(如AuNCs@Ti3C2Tx),材料抑制效果显著降低。
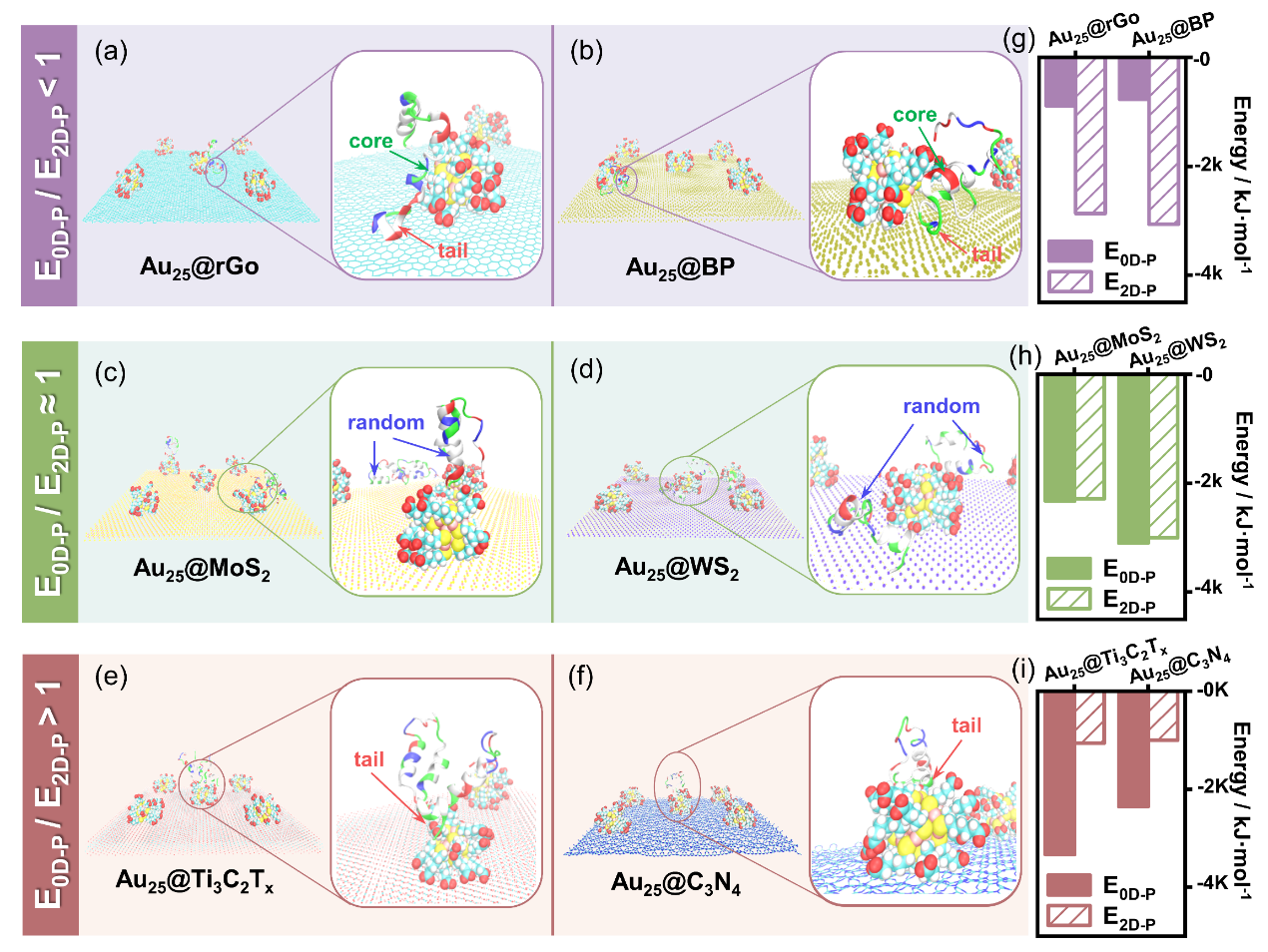
不同非共价界面亲和能比值(E0D-p/E2D-p)的NPs@NSs对淀粉样蛋白行为的影响
研究团队通过实验验证了上述准则:一方面从抑制蛋白单体纤维化角度,与AuNCs@rGO共孵育的Aβ40单体72小时后仍保持天然构象,纤维化程度降低92%;另一方面从拆解成熟纤维角度,同等条件下,AuNCs@rGO可将成熟纤维的β-折叠含量从81%降至50%,且新型材料AuNCs@BP展现出更强的分解能力。更重要的是,AuNCs@BP在100 mg/L浓度下对神经细胞(PC-12)和人类星形胶质细胞(HA)无毒性,并显著提升Aβ损伤细胞的存活率。
通讯作者高冠斌教授指出:“我们的研究首次建立了纳米复合材料界面能量与淀粉样蛋白调控功能的量化关系。这一准则不仅适用于阿尔茨海默病,还可扩展至其他淀粉样蛋白相关疾病(如帕金森病)的纳米药物开发。”该成果已通过多种体外模型验证,下一步将探索其在动物体内的代谢与疗效。
神经退行性疾病纳米医药湖北省重点实验室的硕士生慕庆雪为该论文的第一作者,高冠斌教授、沈雷教授和孙涛垒教授为共同通讯作者。本研究获国家自然科学基金项目(52273110, 52372271)、国家高层次人才特殊支持计划和湖北省青年拔尖人才计划支持。论文详细数据参见《Chemical Engineering Journal》第507卷(2025年),论文编号160577。
文章信息:Qingxue Mu, Guanbin Gao*, Zijun Zhang, Bin Zhang, Zhenhua Gu, Xinglin Liu, Liangchong Yu, Lei Shen*, Taolei Sun*. A validated criterion for engineering 0D@2D nanocomposite to modulate amyloid peptide self-assembly and fibril disassembly[J]. Chemical Engineering Journal, 2025, DOI: 10.1016/j.cej.2025.160577
文章链接:https://www.sciencedirect.com/science/article/pii/S1385894725013981
这项研究为精准设计抗淀粉样蛋白纳米药物提供了全新范式,标志着纳米医学在神经退行性疾病治疗领域迈出重要一步。随着后续临床转化研究的推进,这一发现或将为全球数千万阿尔茨海默病患者带来曙光。

